Tecnologia•5 min de leitura
O segredo da longevidade? O tubarão da Gronelândia tem algumas pistas no seu ADN


Um tubarão que nasceu quando Rembrandt pintava os seus primeiros quadros continua a nadar hoje nas profundezas do Ártico. Isso já sabíamos. O que não sabíamos é como.
Duas equipas de investigação, uma liderada pela Universidade de Tóquio e outra pelo Instituto Leibniz de Envelhecimento na Alemanha, publicaram as análises genómicas mais completas do tubarão da Gronelândia (Somniosus microcephalus) até à data, e as descobertas apontam para um mecanismo que a biologia animal não tinha documentado com esta clareza: um sistema de reparação do ADN tão sofisticado que o animal chega aos 400 anos com a retina intacta e sem sinais de degeneração celular.

O que descobriram num genoma o dobro do tamanho do humano
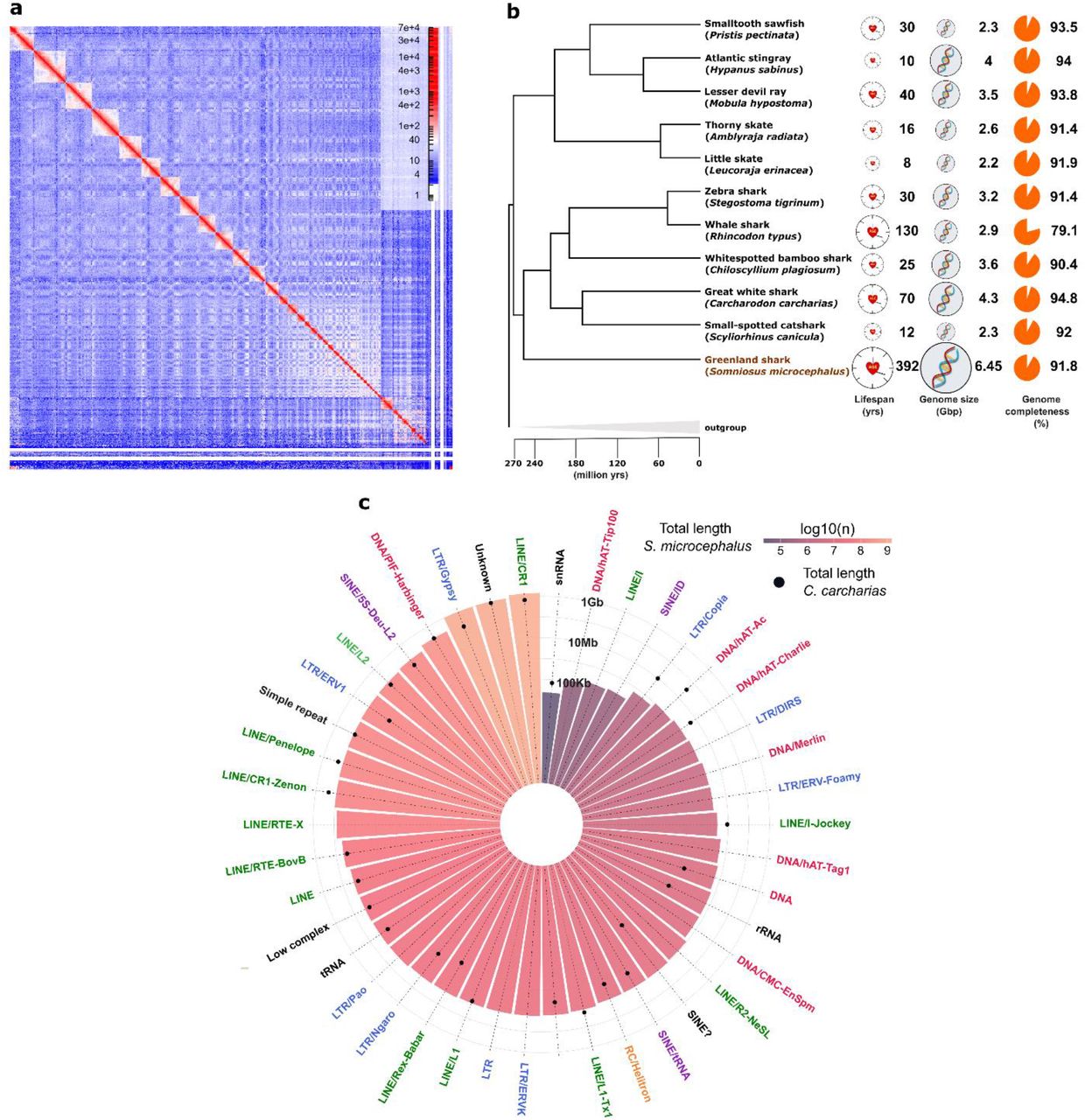
O genoma do tubarão da Gronelândia mede 6,45 gigabases, o que o torna num dos maiores genomas não-tetrápodes sequenciados até agora. Para colocar em perspetiva: o genoma humano ronda os 3,2 gigabases. O do tubarão tem mais do dobro.
Ao analisar as duplicações genéticas, os investigadores encontraram 81 genes que existem como cópia única em todos os outros membros dos elasmobrânquios, a subclasse que inclui tubarões e raias, mas que no tubarão da Gronelândia aparecem duplicados. Segundo a análise funcional, esses genes formam uma rede interligada enriquecida em funções de reparação de quebras de cadeia dupla de ADN.
Isto não é um detalhe menor. As quebras de cadeia dupla são o tipo mais perigoso de dano no ADN: se não forem reparadas corretamente, produzem mutações que derivam em cancro ou morte celular. Na maioria dos vertebrados, a acumulação desse dano com o tempo é, literalmente, o envelhecimento.
Estudos sobre o sistema visual do tubarão confirmaram que a espécie conserva o gene ercc1, que os tubarões de vida mais curta perderam, e exibe níveis elevados de expressão do gene ercc4 em comparação com outras espécies do grupo. Esses dois genes formam o complexo ERCC1-XPF, uma maquinaria de reparação que atua como serviço de manutenção de alta precisão sobre o tecido celular.
O resultado prático: a retina do tubarão mantém a sua funcionalidade durante séculos sem sinais de degeneração, adaptada a condições de luz mínima, o que desafia as suposições sobre a perda inevitável de visão associada ao envelhecimento nos vertebrados.
O gene supressor de tumores com uma mutação que ninguém tinha visto
Há um detalhe que os investigadores do Instituto Leibniz destacam acima dos restantes.
O gene TP53, responsável por suprimir tumores e coordenar a reparação do ADN, aparece como cópia única no tubarão da Gronelândia, sem se duplicar como os restantes. No entanto, essa cópia única transporta uma inserção específica da espécie na sua região C-terminal, uma mutação que não foi observada em nenhum outro elasmobrânquio.
Os modelos computacionais preveem que essa alteração possa modificar a estrutura funcional da proteína p53 e a sua capacidade de gerir o dano genético. Poderia ser, por outras palavras, o interruptor que regula tudo o resto. Mas os próprios autores advertem que se trata de previsões: confirmá-las requer experiências em cultura celular que ainda não foram realizadas.
O que isto não vai fazer por nós
Vale a pena parar aqui um segundo.
"O objetivo não é fazer com que as pessoas vivam mais tempo; o objetivo é manter as pessoas mais saudáveis durante mais tempo", explicou Paul Robbins, biólogo molecular da Universidade de Minnesota, que não participou nos estudos, à National Geographic.
Os tubarões estão demasiado afastados evolutivamente dos humanos e os nossos sistemas são demasiado diferentes para fazer comparações diretas, segundo os próprios investigadores do estudo da National Geographic. O genoma do tubarão não é um roteiro para os 400 anos humanos. É, antes, um catálogo de soluções evolutivas que a biologia ensaiou durante milhões de anos e que poderão iluminar que caminhos existem, não qual tomar.
A utilidade real está na oncologia e nas doenças neurodegenerativas: se se entender porque é que o mecanismo ERCC1-XPF mantém o tecido da retina intacto durante séculos, há bases para procurar intervenções terapêuticas na degeneração macular ou no glaucoma. Se se compreender como a rede de genes duplicados suprime tumores, há pistas para novas estratégias farmacológicas.
O problema do coração
Aí reside a ironia do assunto.
Investigadores que estudam o coração do tubarão da Gronelândia descobriram que este órgão acumula sim as cicatrizes e tensões típicas que o tempo tatua sobre os tecidos. O mesmo animal que mantém a sua retina imaculada aos 400 anos tem um coração que envelhece de forma reconhecível.
Isso sugere que o sistema de reparação de ADN não opera de forma uniforme em todos os tecidos. Alguns órgãos aproveitam-no; outros, nem por isso. A longevidade do tubarão da Gronelândia não é um escudo total contra o tempo. É uma coleção de adaptações muito específicas, desenvolvidas em nichos concretos do organismo, durante centenas de milhões de anos de evolução nas profundezas geladas do Atlântico Norte.
O gene de reparação de ADN tem atuado neste animal como um "gene saltador", dispersando-se no genoma e atrasando a deterioração celular SevenPonds naquilo que os investigadores descrevem como um processo onde o dano potencial dos elementos transponíveis não só se neutraliza, mas pode ser revertido em benefício da integridade genómica.
A pergunta que fica no ar, e que nenhum laboratório ainda respondeu, é quantas dessas adaptações poderiam reproduzir-se farmacologicamente em tecidos humanos específicos, sem necessidade de esperar outros 400 milhões de anos de evolução.
Fontes
As notícias mais importantes enquanto você aprecia um café.
Junte-se à nossa comunidade. Receba nossa análise semanal exclusiva antes de todos.
Notícias Relacionadas

TecnologíaGlobal
5 min de leitura
A NASA confirma a data e a ementa da Artemis II
A nave Orion não tem frigorífico nem reabastecimento. Por isso a NASA preparou 189 artigos únicos, amaranto como proteína, cinco tipos de molho picante e 43 chávenas de café para 10 dias em redor da Lua.

TecnologíaDinero
6 min de leitura
A Meta despede 16.000 pessoas. As suas ações sobem 3%
A Reuters confirmou os planos de corte de até 20% na força de trabalho da Meta. Wall Street celebrou a notícia com uma subida de 3%. Em 2026, a IA já justifica 55.775 despedimentos no setor tecnológico.

Tecnología
6 min de leitura
A Intel prometeu o mesmo há 18 meses. Agora regressa com mais núcleos, preço mais baixo e um truque de software
O Core Ultra 7 270K Plus chega com 24 núcleos e 5,5 GHz por 299 dólares a 26 de março. A verdadeira novidade não está no silício, mas sim numa ferramenta que reescreve o código dos jogos em tempo real para favorecer a Intel.











